手性是自然界的基本属性,手性合成是有机化学、材料化学、药物化学及催化等多个领域最为重要研究内容之一。其中,不对称催化使用少量的手性源实现不对称扩增,是不对称合成领域的核心和难点。近日,东北师范大学在该领域取得了突破性研究进展。
硝酮是一类极为重要的有机化合物,在生物医药、自由基化学、聚合物工业等领域有重要的直接应用价值,在有机合成领域被广泛用于构建各种重要的杂环化合物和天然产物。然而,目前催化合成硝酮的方法较少,且尚无高对映选择性的催化转化。近期东北师范大学有机化学学科的研究团队发展了Cu(I)催化的肟与环丙烯衍生物高对映选择性合成对映体富集的环丙基硝酮衍生物的新方法。作为肟的第一例分子间Cope-型氢胺化反应,该反应具有原料和催化剂廉价易得、原子经济性高等优势。同时,这一机理新颖的高效催化策略也提供了首例高对映选择性的硝酮形成方法,为手性硝酮的催化合成提供了广阔的前景 (图一)。该研究工作由张前教授、赵金钵副教授指导,2016级博士研究生李占宇等同学共同完成,发表于化学权威期刊《美国化学会志》上(Asymmetric Nitrone Synthesis via Ligand-Enabled Copper-CatalyzedCope-Type Hydroamination of Cyclopropene with Oxime, J. Am. Chem. Soc. 2017, 139, 11702-11705).
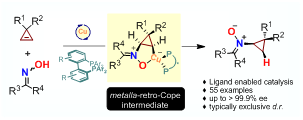
图一
过渡金属催化的对映选择性烯丙基取代反应可在分子中引入重要的烯丙基官能团的同时构建立体中心,在有机合成、药物设计以及材料化学领域应用广泛。然而,该方法常用金属有机试剂(例如:格氏试剂、有机锂试剂、有机锌试剂或有机硼试剂)仍存在官能团兼容性差、制备步骤繁琐、稳定性差及不易储存等缺点。最近,该团队以现场产生催化量的金属有机中间体替代传统化学计量或超过化学计量的金属有机试剂,发展了首例直接以廉价、易得及稳定的炔烃为原料的对映选择性烯丙基化反应,该方法可以通过配体调控实现高化学、区域及对映选择性地获得支链型(SN2’)及线性(SN2)的目标产物(图二)。该研究工作由张前教授、熊涛副教授指导,2015级博士研究生徐国兴等同学共同完成,发表于化学权威期刊德国《应用化学》上(Ligand-Controlled Regiodivergent and Enantioselective Copper-Catalyzed Hydroallylation of Alkynes, Angew. Chem. Int. Ed. 2017, 56, 13130-13134).
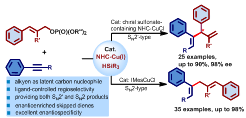
图二
上述高水平研究论文的发表标志我校有机化学学科开辟了不对称催化的新方向,目前,该研究团队还在进行更为深入的研究,有望在不久的将来取得更好的研究进展和成果。